Isomer, IX IPA 2
Mapel : Kimia
Guru B. Study : Siti Maysaroh, s.Pd
Kelas : XI IPA 2
Materi : Isomer
Tujuan pembelajaran: peserta didik dapat menuliskan dan menggolongkan ke dalam isomer struktur dan isomer geometri
ISOMER
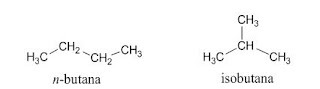
Di antara senyawa-senyawa organik yang telah diketahui di alam ini, ternyata banyak ditemukan senyawa-senyawa berbeda yang mempunyai rumus molekul sama. Sebagai contoh senyawa n-butana (CH3CH2CH2CH3) dan 2-metilpropana (CH3CH(CH3)CH3), kedua senyawa berbeda tersebut memiliki rumus molekul yang sama, yaitu C4H10. Butana merupakan komponen utama elpiji, bahan bakar kendaraan roda dua, dan bahan baku pembuatan karet sintetis. Pada umumnya pematik api gas diisi dengan n-butana dan 2-metil-propana. Butana memiliki titik didih 0,5oC sedangkan 2-metilpropana memiliki titik didih -10,2oC. Butana adalah isomer dari 2-metilpropana, dengan kata lain butana dan 2-metilpropana adalah senyawa-senyawa yang berisomer.
PENGERTIAN ISOMER
Isomer adalah gejala atau peristiwa terdapatnya beberapa senyawa berbeda yang mempunyai rumus molekul sama. Senyawa-senyawa yang berisomer dikatakan merupakan isomer satu sama lain. Fenomena terdapatnya senyawa yang berbeda tetapi memiliki rumus molekul yang sama yaitu n-butana dan 2-metil-propana merupakan gejala isomer.
Isomer adalah suatu senyawa dari beberapa senyawa yang mempunyai rumus molekul sama, tetapi mempunyai sifat berbeda akibat perbedaan susunan atom-atomnya. Dengan kata lain, isomer adalah suatu senyawa dari beberapa senyawa berbeda yang mempunyai rumus molekul sama. Kata isomer berasal dari kata Latin isomeres yang berarti mempunyai bagian yang sama. Isomeres sendiri merupakan gabungan dari kata iso yang artinya sama, dan meros yang artinya adalah bagian.
Kedua senyawa tersebut jelas merupakan senyawa yang berbeda, hal tersebut diketahui dari struktur dan sifat kedua senyawa yang berbeda. Senyawa 1-butena merupakan senyawa dengan rantai karbon terbuka dan mempunyai gugus fungsi berupa ikatan rangkap dua, sedangkan siklobutana merupakan senyawa dengan rantai karbon tertutup atau siklis dan tidak mempunyai ikatan rangkap dua. Senyawa 1-butena berwujud gas pada suhu kamar, karena mempunyai titik didih- 5oC, sedangkan siklobutana berwujud gas, atau dapat berupa cairan pada daerah bersuhu rendah (yaitu yang mempunyai suhu kamar kurang dari 13oC). Senyawa 1-butena mempunyai rumus molekul C4H8, dan siklobutana juga mempunyai rumus molekul sama, C4H8. Karena kedua senyawa merupakan senyawa berbeda tetapi mempunyai rumus molekul sama, maka 1-butena dan siklobutana berisomer.
Struktur 2-butena adalah CH3CH=CHCH3. Senyawa ini berbeda dengan 1-butena karena letak ikatan rangkap duanya berbeda, dan berbeda dengan siklobutana karena rantai karbonnya terbuka, sedangkan siklobutana tertutup. Akan tetapi, 2-butena mempunyai rumus molekul yang sama dengan 1-butena atau siklobutana, yaitu C4H8. Dengan demikian 2-butena adalah isomer dari 1- butena dan siklobutana.
Bila diperhatikan lebih lanjut, ternyata terdapat dua jenis 2-butena, yaitu :
Cis-2-butena dan trans-2-butena berbeda dalam susunan gugus atau atom yang terikat pada karbon ikatan rangkap, pada cis-2-butena gugus-gugus metil terikat pada sisi ikatan rangkap yang sama, sedangkan pada trans-2-butena gugus-gugus metil terikat pada sisi ikatan rangkap yang bersebrangan. Perbedaan struktur keduanya menyebabkan sifat keduanya juga berbeda, salah satunya dapat ditunjukkan dari titik didih cis-2-butena dan trans-2-butena yang berbeda. Dengan demikian, cis-2- butena dan trans 2-butena merupakan isomer satu sama lain.
JENIS-JENIS ISOMER
Terdapat dua jenis isomer, yaitu isomer struktur dan stereoisomer. Isomer struktur terjadi pada senyawa-senyawa yang memiliki rumus molekul sama, namun berbeda ikatan antar atom-atomnya., sedangkan stereoisomer adalah isomer dengan perbedaan terletak pada cara penataan atom-atom dalam ruang, tetapi urutan penggabungan atom-atomnya tidak berbeda.
Terdapat tiga jenis isomer struktur, yaitu isomer rantai, fungsional dan posisi.
a. Isomer rantai adalah gejala terdapatnya beberapa senyawa yang berumus molekul sama, tetapi mempunyai rantai karbon berbeda.
b. Isomer posisi terjadi pada senyawa-senyawa yang memiliki rumus molekul sama, namun berbeda letak atau posisi gugus fungsi atau substituennya.
c. isomer gugus fungsional adalah senyawa dengan rumus molekul sama, namun berbeda gugus fungsinya.
Isomer ruang dibedakan menjadi dua, yaitu isomer geometri (dalam konteks bidang dua-dimensi) dan isomer optik (dalam konteks ruang tiga-dimensi).
a. Isomer Geometri (cis-trans)
Isomer geometri didefinisikan sebagai peristiwa terdapatnya beberapa senyawa berbeda yang mempunyai rumus molekul sama, dan perbedaan di antara senyawa-senyawa tersebut terletak pada cara penataan gugus-gugus di sekitar ikatan rangkap. Isomer geometri diakibatkan oleh ketegaran dalam molekul, yang dijumpai dalam dua golongan senyawa, yaitu: alkena dan senyawa siklik. atom atau gugus atom yang terikat dengan ikatan rangkap tidak dapat berputar bebas, sehingga alkena menampakkan gejala isomer geometri. Contohnya adalah cis-1-butena dan trans
Isomer optik adalah gejala isomer yang terjadi akibat perbedaan arah bidang putar cahaya terpolarisasi.
· Khiralitas
Suatu objek yang tidak dapat diimpitkan pada bayangan cerminnya dikatakan kiral






Komentar
Posting Komentar