Kelas 11 IPS 1, pert ke 2 Bab Alkana, alkena dan alkuna
SENYAWA HIDROKARBON
Perbedaan alkana, alkena dan alkuna dilihat dari rumus umum, akhiran nama, dan struktur ikatan
Nama guru b. study : siti Maysaroh, S.Pd
Mata Pelajaran : Kimia
Materi Pokok : Senyawa hidrokarbon dan jenis-jenisnya
Assalamualikum anak-anaku sekalian..
Bagaimana kabar kalian? semoga kalian semua dalam keadaan baik dan terjaga sholat 5 waktunya diawal waktu ya...., dan jangan lupa untuk selalu mengerjakan sholat duha secara istiqomah ya sebelum memulai pjj kalian.
Hari ini kita akan melanjutkan materi yang sebelumnya ya yaitu masih tentang hidrokarbon. Diharapkan kalian dapat membedakan senyawa alkana, alkena, dan alkuna dilihat dari struktur ikatan dan penamaan senyawanya.
Untuk hari ini tugas kalian yang ke
1. Pahami isi materi berikut ini
2. Lengkapilah tabel alkana, alkena dan alkuna sampai jumlah atom C nya 10 yang ada dibagian bawah materi berikut ini.
3. Buat ringkasan tentang materi hari ini ( perbedaan alkana, alkena dan alkuna)dan kumpulkan hasil ringkasan materi kalian dalam bentuk screanshot ke email siti.alazhar3@gmail.com
Materi:
1. Kekhasan Atom Karbon
Atom karbon mempunyai nomor atom 6, dengan 4 elektron valensi. Atom karbon dengan keempat tangan ikatan itu dapat membentuk rantai atom karbon dengan berbagai bentuk dan kemungkinan. Semakin banyak jumlah atom karbon atau semakin panjang rantai karbon, semakin banyak jenis senyawa yang bisa dibentuk oleh atom karbon.
Beberapa kemungkinan rantai karbon yang dibentuk dapat dikelompokkan berdasarkan jumlah ikatan dan bentuk rantai. Berdasarkan jumlah ikatan yaitu ada
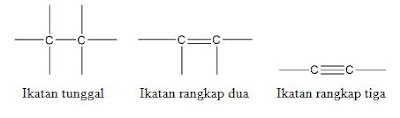
1. ikatan tunggal yaitu ikatan antara atom - atom karbon terdapat ikatan
2. ikatan rangkap dua yaitu ikatan antara atom - atom karbon terdapat ikatan
3. ikatan rangkap tiga yaitu ikatan antara atom - atom karbon terdapat ikatan
Berdasarkan bentuk rantai, ada
1. Rantai terbuka (alifatis) yaitu rantai antar ujung-ujung atom karbon tidak saling berhubungan. Rantai terbuka terdapat rantai lurus (tidak bercabang) dan rantai bercabang.
2. Rantai tertutup (siklis) yaitu terdapat pertemuan antara ujung-ujung rantai karbonnya. Terdapat 2 jenis dalam rantai ini alisiklis dan aromatis. Rantai alisiklis adalah rantai tertutup dan tidak memiliki ikatan berkonjugasi (selang – seling ikatan tunggal dan ikatan rangkap) sedangkan rantai aromatis adalah rantai tertutup yang memiliki ikatan berkonjugasi (selang – seling ikatan tunggal dan ikatan rangkap)
1. Hidrokarbon
Kelompok senyawa karbon yang paling sederhana adalah hidrokarbon, yaitu senyawa karbon yang tersusun dari atom karbon dan hidrogen. Berdasarkan bentuk rantai karbonnya Senyawa hidrokarbon dibedakan sebagai berikut :
1. Senyawa hidrokarbon alifatis adalah senyawa hidrokarbon rantai antar ujung atom karbon tidak saling berhubungan.
2. Senyawa hidrokarbon siklis adalah senyawa hidrokarbon rantai tertutup dan tidak memiliki ikatan berkonjugasi (selang – seling ikatan tunggal dan ikatan rangkap). Contohnya sikloheksana dan sikloheksena.
3. Senyawa hidrokarbon aromatis adalah rantai tertutup yang memiliki ikatan berkonjugasi (selang – seling ikatan tunggal dan ikatan rangkap). Contoh hidrokarbon aromatik yaitu benzena, naftalena ( kapur barus), dan toluena.
Berdasarkan ikatan yang terdapat ada rantai karbonnya, hidrokarbon dibedakan menjadi:
Hidrokarbon yang seluruh ikatan antar karbonnya semua ikatan tunggal maka disebut kelompok alkana. Hidrokarbon yang mengandung ikatan rangkap dua disebut alkena dan hidrokarbon yang mengandung ikatan rangkap tiga disebut alkuna.
a. Alkana
adalah hidrokarbon jenuh dengan semua ikatan antar atom karbonnya merupakan ikatan tunggal. Rumus umum alkana yaitu : CnH2n+2 ; n = jumlah atom C.







Shanaya Aulia Irvan
BalasHapusXI IPS 1
Aisyah Nur Jannah
BalasHapusXI IPS 1
Cut Yusi Ratu Aulia
BalasHapusXI IPS 1
Sihab wildan
BalasHapusXI IPS 1
friza aqif arafi
BalasHapusxi ips 1
Komentar ini telah dihapus oleh pengarang.
BalasHapusRaditya tri w
BalasHapusXI IPS 1
Kurniawan Sidiq
BalasHapusXI IPS 1
yolanda febri mulia putri
BalasHapusXI IPS 1
Achmad Nugraha Ramadhani
BalasHapusXI IPS 1
Andrean prayoga
BalasHapusXI IPS 1
Dimas Farevi Abdullah
BalasHapusXI IPS 1
Annisa Dwi Handayani
BalasHapusXI IPS 1
Elnisa Aurra
BalasHapusXI IPS 1
Kenovadya Andam
BalasHapusXI IPS 1
Firda irma dela putri
BalasHapusXI IPS 1
Tiara Eka Putri
BalasHapusXI IPS 1
Bintang Anugrah
BalasHapusXI IPS 1
Muhammad Afgan Shaq
BalasHapusXI IPS 1