Kelas 10 IPA2, Konsep mol
Konsep Mol, Massa Molar dan Volume Molar
Diperlukan suatu konversi yang menghitung jumlah partikel
yang kita ukur. Dalam ilmu kimia, konversi tersebut dikenal dengan mol. Satu
mol
didefinisikan sebagai banyaknya suatu zat (gram/L) yang mengandung identitas
dasar berupa atom, mol, atau partikel lain sebanyak atom yang terdapat dalam 12
gram atom C-12, sedangkan massa
1 atom C-12 adalah 1,999268
x 10-23
Jadi standar mol adalah 12 gram C-12. Melalui berbagai
percobaan, Loscmith menemukan Jumlah partikel yang
terdapat dalam 12 gram atom C-12 yaitu:
Artinya, bahwa
dalam 1 mol terdapat 6,02
x 1023partikel, yang
selanjutnya disebut bilangan Avogadro yang dinyatakan dengan lambang L.
Terdapat hubungan
jumlah mol dengan jumlah partikel yaitu
sebagai berikut:
Jumlah
partikel = jumlah mol x bilangan Avogadro
n = mol
Sedangkan hubungan
mol dengan massa zat yaitu sebagai
berikut:
n= mol,
mm= masa molar atau Mr
Contoh:
1. Untuk membuat 2 mol urea diperlukan berapa gram pupuk urea? Jika diketahui masa molekul relatif urea adalah 60.
Jawab:
massa = mol x Mr
= 2 x 60
= 120 gram
2. Dalam 50 gram HF, terdapat berapa molkah senyawa HF tersebut Jika diketahui Mr HF=19.
Jawab:
massa = Mol x Mr
Mol = massa/ Mr
= 50 /19
=2,63 mol
UJI KEPAHAMAN:
1. Tentukanlah mol dari 80 gram sukrosa, Mr sukrosa adalah 180.
2. Tentukan massa garam NaCl yang terdapat dalam 3 mol garam dapur teesebut, jika Mr NaCl adalah 58,5






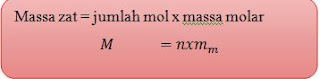



Vadia Camila
BalasHapusX IPA 2
Fitri gautari
BalasHapusX IPA 2
Nia aprilliana
BalasHapusX IPA 2
Tami Aurelia Putri
BalasHapusX IPA 2
Ravi Andradisa Athallahfaiq
BalasHapusX IPA 2
prema kusherawati
BalasHapusx ipa 2
Mira Tantia
BalasHapusX IPA 2
Winda Oktavia
BalasHapusX ipa 2
anisa nurul vania
BalasHapusNanda nishappy permata rindu
BalasHapusX IPA 2