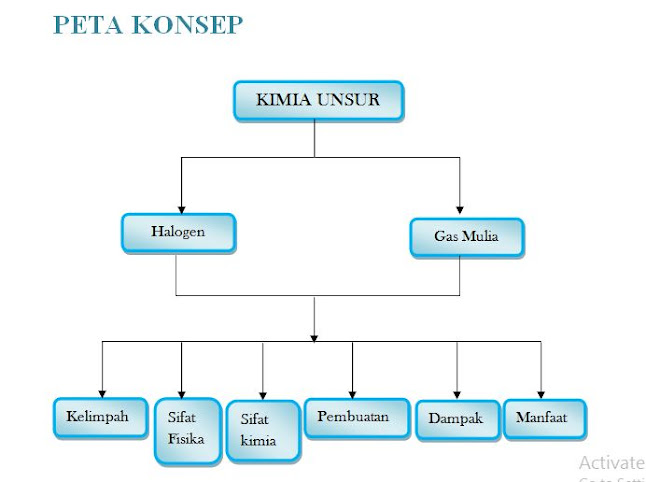
Tanpa kita sadari, kita sering menggunakan baik makanan, obat-obatan, peralatan yang terbuat dari suatu unsure. Baik yang merupakan unsure logam maupun unsure non logam. Salah satu contoh unsure yang dialam dalam bentuk senyawaan adalah unsure halogen, yaitu klor yang terdapat dalam bahan pemutih pakaian, sedangkan yang berada dialam dalam bentuk monoatomik adalah unsure gas mulia, yaitu gas neon yang terdapat dalam bohlam lampu. Selain mempelajari kelimpahan unsure dialam, kalian juga akan mempelajari sifat fisika dan kimia, proses pembuatan, dampak serta manfaat dalam kehidupan sehari-hari dari setiap unsure. Unsur-Unsur Halogen Tahukah kamu, apa itu halogen? Secara harfiah halogen berarti pembentukan garam, hal ini sesuai dengan fakta bahwa unsure-unsur golongan halogen dapat menghasilkan garam, yaitu jika bereaksi dengan logam-logaM, terutama logam alkali dan alkali tanah. Kelimpahan unsur merupakan keberadaan unsur-unsur yang ada dikulit ...